Affiner toujours plus les connaissances sur les cancers du sein
L’oncogenèse mammaire est un processus complexe. Depuis une dizaine d’années, chercheurs et cliniciens spécialistes du cancer du sein ont mis en évidence des mécanismes moléculaires et des anomalies génétiques associées à l’apparition et au développement de la maladie, ainsi qu’à la gène HER2. Mais dans certains cancers du sein, ce nombre de copies se retrouve en excès, ce qui aboutit à une accumulation de la protéine correspondante : on dit que HER2 est surexprimé et on parle d’un cancer du sein HER2 positif. Or la surexpression de HER2 est un facteur de survie de la cellule cancéreuse : l’anomalie favorise la croissance de la tumeur et la rend particulièrement virulente.
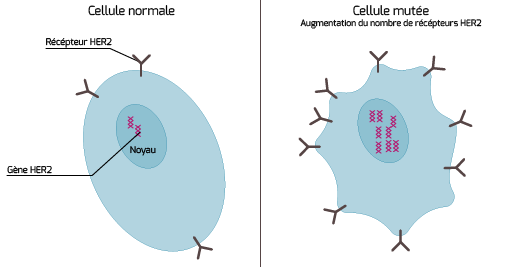
HER2 Positif – Institut National du Cancer (INCa)[/caption]
En mettant en évidence le rôle de HER2 dans ce cas particulier, la biologie a, de fait, permis le développement d’un médicament ciblé : trastuzumab / Herceptin®. Cet anticorps monoclonal spécifique reconnaît la cible HER2 à la surface des cellules cancéreuses positives, vient s’y fixer, perturbe le mécanisme impliqué dans la prolifération et « recrute » le système immunitaire de la patiente pour détruire les cellules reconnues. Depuis, d’autres thérapies ciblées anti HER2 ont été commercialisées.
Une piste pour augmenter le taux de guérison : les cellules à l’origine de la maladie ou cellules souches
Voie particulièrement originale et innovante, la recherche sur les cellules souches cancéreuses est porteuse de grands espoirs pour l’avenir. Cellules à partir desquelles s’amorcerait le processus « d’initialisation » du cancer (cancérogenèse), les cellules souches cancéreuses seraient en effet à l’origine de la maladie.
Elles joueraient également un rôle majeur dans la résistance au traitement et la persistance de la tumeur, mais aussi dans le développement des métastases et la survenue de rechutes. Car si les traitements parviennent le plus souvent à éliminer les cellules tumorales, ils sont de fait encore souvent incapables de tuer ces cellules mères immatures qui risquent à tout moment de donner naissance à une nouvelle tumeur : certaines de leurs caractéristiques, très différentes de celles des cellules tumorales plus différenciées, les rendent insensibles à la plupart des traitements et leur permettent de résister à des conditions physiologiques extrêmes.
L’IPC fait partie des équipes-phares, reconnues pour leur travail sur les cellules souches cancéreuses du cancer du sein. Le groupe de recherche spécifiquement dédié à l’étude des cellules souches cancéreuses mammaires est parvenu à isoler ces cellules à l’origine de la maladie et à caractériser leurs spécificités.
Ces cellules souches très résistantes aux traitements représentent moins de 0,1 % des cellules qui composent une tumeur. Trouver des traitements efficaces sur ce petit contingent permettrait, non seulement de soigner totalement le cancer du sein, mais aussi d’anticiper, voire de prévenir, les récidives et d’offrir aux cancers métastatiques des perspectives thérapeutiques. Des essais de phase précoce, concernant notamment des voies métaboliques dans ces cellules souches, ont déjà démarré à l’IPC.
Comprendre les mécanismes d’échappement de la tumeur face au système immunitaire et les contrer grâce à l’immunothérapie
Mieux comprendre les stratégies qu’utilisent les cellules tumorales pour échapper aux cellules immunitaires qui les combattent permet de développer de nouveaux médicaments, des traitements d’
Là encore, il s’agit de redonner au système immunitaire défaillant des armes pour se battre de nouveau contre le cancer. En l’occurrence, en réactivant grâce à un vaccin les cellules du système immunitaire missionnées pour reconnaître des antigènes surexprimés dans les tumeurs. Enfin, la transplantation de « cellules tueuses » fonctionne un peu sur le même principe. Pour contrecarrer le fait que les cellules cancéreuses parviennent à empêcher les cellules tueuses du système immunitaire de les reconnaître et prospèrent ainsi « incognito », une troisième stratégie consiste à prélever ces cellules immunes chez le patient. Elles sont ensuite modifiées génétiquement, c’est-à-dire en quelque sorte « rééduquées », puis réinjectées au malade pour reprendre leur fonction initiale de défense.Le vaccin thérapeutique, transplantation de « cellules tueuses », modification génétique des cellules immunes du patient : d’autres voies de recherche porteuse d’espoirs ?
La montée en puissance des technologies de séquençage
L’accélération de toutes ces retombées va de pair avec l’avènement des séquenceurs à haut débit, grâce auxquels il est devenu possible de caractériser les altérations d’une tumeur. C’est-à-dire d’établir le statut de l’ensemble des gènes (génomique). Chaque tumeur peut en effet comporter des anomalies spécifiques sur un nombre plus ou moins grand de gènes.
L’IPC dispose aujourd’hui de trois séquenceurs de nouvelle génération : deux sont dédiés à la recherche, le troisième sert déjà au diagnostic. Il est donc désormais envisageable, dans un délai allant de quelques jours à quelques semaines, compatible avec la prise en charge personnalisée des patientes, d’obtenir une cartographie quasi complète, individualisée, des altérations présentes dans leur tumeur.
Vers les « biopsies liquides » ?
Une autre technique, très innovante mais qui n’en est qu’à ses balbutiements, est à l’étude : l’analyse, après une simple prise de sang, des altérations présentes dans le sang. L’idée consiste à extraire et à analyser l’ADN tumoral ou les cellules tumorales circulantes. Cette nouvelle approche, alternative aux biopsies traditionnelles, pourrait permettre, à partir du « reflet » de la tumeur dans le sang circulant, de mieux l’évaluer, d’apprécier son agressivité, de suivre l’éventuelle apparition de nouvelles anomalies, par exemple en cas d’apparition de métastases, et ainsi de mieux piloter les traitements dits ciblés.
Au regard du nombre d’anomalies caractéristiques des cancers du sein, cette approche offre a priori peu d’intérêt au niveau du dépistage face à la mammographie. En revanche, son développement pourrait s’avérer profitable pour le suivi de la maladie et l’évaluation d’une éventuelle rechute. L’IPC participe à des essais thérapeutiques visant à évaluer le bénéfice de la recherche de cellules tumorales et de l’analyse de l’ADN tumoral circulant dans le sang auprès de patientes atteintes d’un cancer du sein métastatique.
Plusieurs types et sous types de cancer du sein : une stratification de plus en plus précise
Parfaire la connaissance de la biologie des cancers du sein a permis aux cliniciens d’améliorer leur classification et de mettre en évidence leur grande hétérogénéité. Aujourd’hui, un cancer du sein se définit, en fonction :
- des cellules à partir desquelles il s’est développé et de sa localisation dans la glande mammaire : grade histologique et du degré d’agressivité de la tumeur ;
- de son statut de maladie localisée ou métastatique.
Mais aussi, en fonction de différents biomarqueurs, entre autres :
- selon la présence ou non de récepteurs hormonaux (œstrogène et/ou progestérone) sur les membranes des cellules tumorales : 70 % des cancers du sein sont « hormono-sensibles » ;
- selon la présence ou non de récepteurs HER2, cible de l’Herceptin® (anticorps monoclonal) : c’est le cas de 15 % à 20 % des cancers du sein, localisés ou métastatiques, diagnostiqués chaque année en France ;
- si le cancer n’exprime pas de récepteurs hormonaux et n’exprime pas HER2, il est dit triple négatif.
Dans leur ensemble, les tumeurs du sein s’avèrent donc extrêmement hétérogènes entre elles. A cette hétérogénéité inter-tumorale s’ajoute par ailleurs une hétérogénéité intra-tumorale, avec la présence de sous-populations de cellules : toutes les cellules ne sont pas identiques entre elles au sein d’une même tumeur. Le tout induit différentes réponses aux traitements, comme dans le cas de maladies différentes, et une autre façon de « penser » les tumeurs. A la clé : de nouvelles stratégies de prise en charge diagnostique et thérapeutique.
Pour autant, si l’oncologie maîtrise aujourd’hui une bonne majorité des cancers du sein, il reste néanmoins des zones d’ombre : les chercheurs et les cliniciens de l’IPC s’attellent notamment à trouver de meilleures approches thérapeutiques pour les cancers du sein localisés mais de sous-type agressif, ou encore les cancers du sein inflammatoires.
